神経膠腫(グリオーマ)、神経膠芽腫(グリオブラストーマ)
組織診断・遺伝子診断による
最新の知見に基づいた治療
昭和医科大学では、昭和医科大学グループ内で連携を取り、各施設間で協力して脳腫瘍の治療を行っています。
昭和医科大学グループでは年間141例(2017年)の脳腫瘍の手術を行っています。
脳腫瘍の中でも多い疾患が神経膠腫(グリオーマ)です。
治療の基本は手術で最大限摘出することですが、グリオーマは手術で摘出を行うだけでは治療が終わらず、放射線治療・化学療法(抗がん剤治療)と併用して治療を行っていきます。しかし、これらの治療を行っても、難治な患者さんが多く存在する脳腫瘍です。
昭和医科大学では標準的な治療だけではなく新しい治療についても積極的に取り入れ、それぞれの患者さんに最も適した医療を提供いたします。
診断・検査について
脳腫瘍に対しては通常CTやMRI検査を行いますが、それらに加えて、fMRI(functional MRI、 機能MRI)やトラクトグラフィー(運動や言語の神経線維を描出し、腫瘍との位置関係を明らかにします)を使用し、障害を出さないように摘出術を行うシミュレーションを行います。また、腫瘍の再発か放射線の治療の変化かを検討する場合には、PET(Positron Emission Tomography)検査の情報も踏まえて検討を行っています。
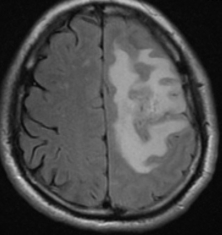
グリオーマの画像:左はMRIのFlair画像、右は造影T1強調画像です。
左の頭頂葉に造影される腫瘍を認め、腫瘍の周囲に脳浮腫を来しています。
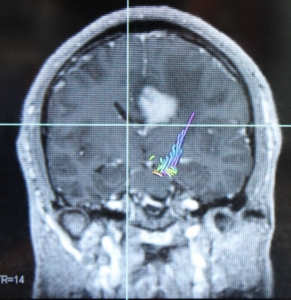
トラクトグラフィー:運動神経の線維をMRI画像の中に描出することで腫瘍との位置関係がわかります。
治療
外科手術
グリオーマは腫瘍をできるだけ摘出したほうが、予後の改善につながるという世界中からの報告があり、最大限の摘出を目指して手術を行います。
手術で簡単に摘出できる腫瘍もありますが、手足の運動神経や言葉・意識に関係する部位に腫瘍ができた場合、手術での摘出は極めて困難になります。摘出することによって麻痺や意識障害・失語などの重篤な合併症が出現してしまった場合、たとえ腫瘍がすべて摘出されたとしても、かえって予後が悪くなることが報告されています。そのような場合には腫瘍の一部だけを取ってくる生検術というものを行うこともあります。
また、当院には神経内視鏡技術認定医が5名在籍しており、内視鏡を使用した低侵襲の手術(生検術)も積極的に行っています。
術中ナビゲーション
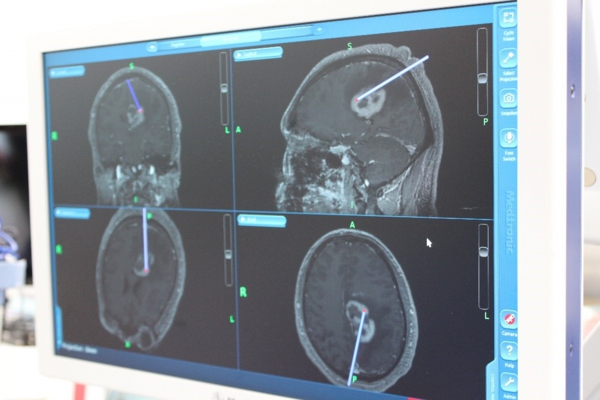
昭和医科大学では術中ナビゲーションを使用した脳腫瘍の手術を行っています。
術前に撮影したCTやMRIの画像を用いて、車のナビゲーションのように、今どの場所を摘出しているのか、またどのくらい摘出できたか(摘出度)を確認でき、より安全に適切な範囲の摘出が可能です。
モニタリング
運動神経・感覚、目の見え方や聴力の中枢に近い場所にできた腫瘍の場合、摘出してしまうと麻痺・感覚障害、視力障害や耳が聞こえなくなってしまう可能性があります。その場合にはリスク軽減のために術中電気生理学的モニタリングを行い、手足の運動機能や視力・聴力を調べながら手術を行います。
ハイブリッド手術室
昭和大学にはハイブリッド手術室と呼ばれる、脳血管撮影が可能な手術室があります。術中に脳血流の評価が必要な場合や、腫瘍への栄養血管を術中に確認する必要がある場合には、脳血管撮影装置を備えた手術室で手術を行います。
5-ALA(アミノレブリン酸)
当院では、5-ALA(アミノレブリン酸)を使用した手術を行っています。手術前に5-ALAというお薬を飲んでいただくと、手術中に特殊な光を当てることで腫瘍が赤く光り、腫瘍と正常脳の境界がわかりやすくなります。通常の手術顕微鏡では境界がわかりづらく、腫瘍を取り残してしまうことがあるため、5-ALAを使用することで腫瘍の摘出度が上がります。
また、腫瘍の一部を取ってくる生検術では、5-ALAを使用することによって、確実に腫瘍である部分を摘出することが可能になります。それにより誤った診断になることを防げます。
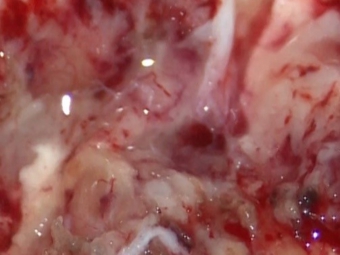
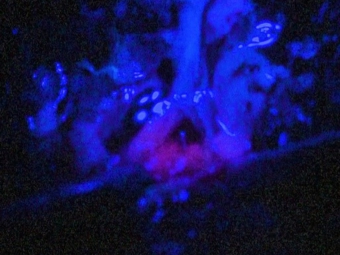
左は通常の顕微鏡の写真。残存している腫瘍は肉眼的には区別が困難ですが、5ALA(右図)を使用することで残存している腫瘍が赤く光って見えます。
これらの機材を適材適所に用いて、より安全に最大限の摘出を行っています。
その後の治療
遺伝子診断に基づいた診断・治療
WHO(世界保健機関)によって、脳腫瘍の分類が2016年に改訂されました。腫瘍に生じている遺伝子異常が診断に役立ち、予後を決める要素であるということがわかってきたため、改訂されたWHO2016脳腫瘍分類では遺伝子情報によってグリオーマが分類されるようになりました。そして、腫瘍の遺伝子異常の型によっては、予後の良好なことが見込まれる患者さんがわかるようになりました。
当院では従来の腫瘍組織診断に加え、IDH変異、1p19q染色体共欠失、MGMTメチル化などの腫瘍の遺伝子変異を調べることで、診断および治療方針の決定の決定に役立てています。
放射線療法
グリオーマは手術だけでは治療が終わらず、手術後に放射線と化学療法が必要になることが多い腫瘍です。
放射線は、一般的には総線量60Gy(グレイ)を6週間かけて腫瘍および腫瘍周囲に照射します。高齢の患者さんに対しては、総線量40Gyを3週間かけて照射することもあります。高齢の患者さんに対しては60Gyを6週間かけて照射した場合と同等の効果が得られ、治療期間が短縮できるとされています。
また、昭和大学では日本臨床腫瘍グループ(Japan Clinical Oncology Group: JCOG)の臨床試験も行っています。
化学療法
テモダール(一般名テモゾロミド)
グリオーマに対する化学療法、いわゆる抗がん剤治療はテモダールを使用するのが標準的です。このお薬は飲み薬であることと、一般的な抗がん剤に比べ副作用が少ないことが特徴です。また点滴の薬もあり、薬が飲めない患者さんへの治療も可能です。放射線治療中は毎日内服し、放射線治療終了後は4週間休薬します。その後1ヶ月に1度外来通院をしていただき、5日間内服して23日休薬するというペースで外来での投与を継続していきます。
アバスチン(一般名ベバシズマブ)
アバスチンとは分子標的薬に分類される薬です。分子標的薬とは、体内の特定の分子をターゲットにした治療のことです。アバスチンは腫瘍に栄養を送る新生血管の増殖を抑える作用があり、腫瘍の増殖を抑える効果があります。日本では初発時・再発時ともに使用ができますが、主に再発時に使われることが多い薬です。
ギリアデル(一般名カルムスチン)

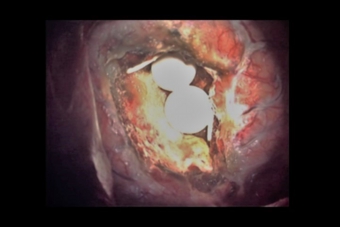
ギリアデルとはカルムスチンという薬が組み込まれている円盤状の抗がん剤です。手術時に腫瘍の摘出腔にこの薬を置いてくると、数週間にわたって薬剤が染み出して効果を発揮します。ただし、広い範囲に薬が広がるわけではないので、腫瘍が肉眼的にすべて摘出されていないと、効果が発揮されません。また、感染や脳浮腫・傷のトラブルが起こる場合があるため、必要な症例に限って使用しています。
再発時の治療
グリオーマは、これまでご紹介したような治療を最大限行っても、再発することが少なくない腫瘍です。再発してしまった場合には、再発時に腫瘍が初発時と変異していることもあるため、可能であれば組織診断を行う目的を兼ねて再手術を行い、できる限り腫瘍を摘出します。初回と同様に再度腫瘍を詳しく調べ、再度放射線治療が可能な場合は、ガンマナイフなどの放射線治療を治療の選択肢としてご提案します。また、使用していない抗がん剤で化学療法を行う場合もあります。
これらの治療を行ってもさらに腫瘍が増大してくる患者さんには、新しい治療(治験・臨床試験)への参加相談・紹介も行っています。
脳腫瘍外来
担当医師/外来日
清水 克悦(しみず かつよし)教授/毎週木曜日
谷岡 大輔(たにおか だいすけ)准教授/毎週火曜日
近 貴志(こん たかし) 助教/毎週火曜日
小林 裕介(こばやし ゆうすけ) 助教/第2・4金曜日
脳腫瘍の手術・化学療法・放射線治療を専門にしています。
これまでに1000件以上の脳腫瘍を経験しております。
脳腫瘍の疾患や治療に関するご相談がございましたら、昭和医科大学病院脳腫瘍外来をお気軽に受診ください。紹介状や予約がなくても対応いたしますが、一人一人の方をしっかり診させていただくため、まずはお電話で予約の確認をお願いします。
医療連携室:(03)3784-8400
